Przygotowywanie leków cytostatycznych - zasady funkcjonowania pracowni
Przygotowywanie leków cytostatycznych jest obowiązkiem aptek szpitalnych. Do usług farmaceutycznych należą m.in. przygotowywanie leków w dawkach dziennych, w tym leków cytostatycznych. Przy wykonywaniu czynności fachowych w aptece (usług farmaceutycznych) mogą być zatrudnieni wyłącznie farmaceuci i technicy farmacji [1,2]. Przygotowane leki cytostatyczne muszą spełniać wymogi stawiane lekom parenteralnym i muszą być wykonywane zgodnie z zasadami Dobrej Praktyki Wytwarzania (GMP) [3,4].

Przygotowywanie leków cytostatycznych musi odbywać się w wydzielonym pomieszczeniu oddzielonym od innych pomieszczeń śluzami. W boksie aseptycznym wymagana jest klasa czystości B oraz min. 10-krotna wymiana powietrza w ciągu godziny [4]. Pomieszczenie to musi być wyposażone w loże przystosowane do pracy z lekami cytostatycznymi. Loże takie są z nawiewem laminarnym i filtrami HEPA. Wewnątrz loży, gdzie odbywa się właściwe przygotowanie leków, wymagana jest klasa czystości A [5,6,7] .
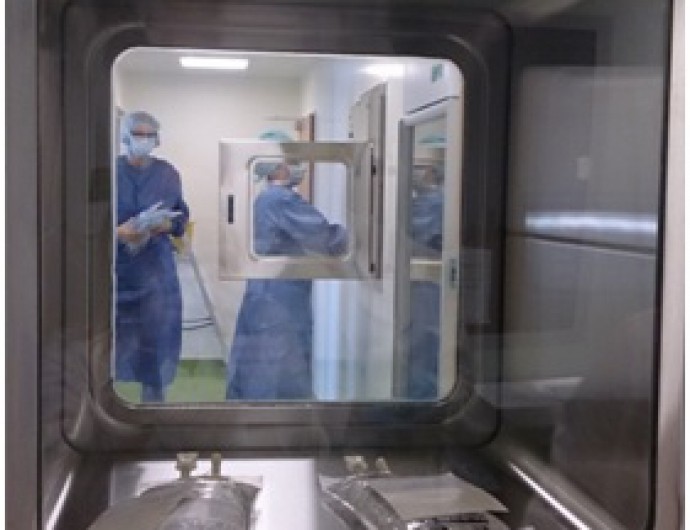
W celu przygotowywania dziennych dawek leków cytostatycznych dla indywidualnych pacjentów apteka szpitalna musi posiadać dobrze przeszkolony i dostatecznie duży zespół pracowników. W pracowni należy unikać stałych stanowisk pracy, a liczba osób narażona na kontakt z lekami cytostatycznymi powinna być minimalna [6]. W tym celu należy wprowadzić zmianowy system pracy. Osoby przygotowujące leki cytostatyczne przebywają w boksach aseptycznych 2 godziny i dopiero po przerwie trwającej minimum 30 minut mogą do niego wrócić [ryc.1]. W czasie przerwy personel wykonuje czynności związane z funkcjonowaniem pracowni, czyli odbieranie gotowych leków, roznoszenie ich na poszczególne oddziały, podawanie m.in.: leków, jałowego sprzętu jednorazowego użytku oraz worków z 0,9% roztworem NaCl lub 5% glukozą [ryc.2]. Zarówno odbieranie gotowych leków cytostatycznych jak i podawanie zdezynfekowanych rzeczy odbywa się poprzez specjalne śluzy [rys.3].
Każdy pracownik wykonujący czynności związane z przygotowywaniem cytostatyków musi stosować indywidualne środki ochrony. Muszą one odpowiadać normom CE (Communaute Europennee). Do indywidualnych środków ochrony należą m.in: jałowy fartuch ochronny najlepiej z wstawkami wodoodpornymi i badaniami na przenikanie cystostatyków, rękawice ochronne przystosowane do pracy z cytostatykami, ochronna maseczka oddechowa oraz ochraniacze na obuwie [6]. Rękawiczki używane podczas produkcji powinny być jałowe i mieć badania na przenikalność cytostatyków. Powinny one być systematycznie zmieniane w trakcie pracy i w przypadku skażenia. W przypadku przygotowywania leku, który ma bardzo krótki czas przenikania przez rękawice, muszą być one niezwłocznie zmienione zaraz po zakończeniu procesu.
Wg QUAPOS 4 : Technika pracy aseptycznej obejmuje wszystkie skoordynowane działania zapewniające jałowość produktu dzięki zastosowaniu optymalnych warunków redukcji skażenia mikrobiologicznego. Odpowiednie przygotowanie i przestrzeganie procesu w istotny sposób wpływa na jakość tego produktu [6]. Każdorazowo przed rozpoczęciem procesu przygotowywania leków: śluzy wejścia i wyjścia, śluzy podawcza i wydawcza, korytarz, boks aseptyczny, stanowisko pracy - stoliki oraz wnętrze loży cytostatycznej muszą być dokładnie umyte odpowiednimi środkami do dezynfekcji. Ponadto podczas przygotowywania leków muszą być zachowane czynności zapobiegające skażeniu mikrobiologicznemu. W boksach aseptycznych znajdują się stojaki z koszyczkami, gdzie przechowywany jest sprzęt jednorazowego użytku oraz worki z 0,9% roztworem NaCl, 5% glukozą oraz butelki z wodą.
Wszystkie preparaty oraz sprzęt medyczny jednorazowego użytku podawany do boksu aseptycznego poprzez śluzę podawczą muszą być dokładnie zdezynfekowane za pomocą 70% spirytusu. By zapobiec kontaminacji podawanych rzeczy do boksu osoby wykonujące powyższe czynności zakładają jałowy fartuch oraz rękawiczki. W celu weryfikacji czystości mikrobiologicznej należy regularnie przeprowadzać odpowiednie badania na obecność mikroorganizmów: badania z użyciem płytek kontaktowych, sedymentacyjnych oraz przeprowadzanie próby ślepej [6,8].
Dzienne dawki cytostatyków dla indywidualnego pacjenta przygotowuje się na podstawie pisemnego zlecenia lekarskiego weryfikowanego przez farmaceutę [6]. Zlecenie powinno zawierać wszystkie dane pacjenta : imię, nazwisko, wiek, wagę, wzrost, powierzchnię ciała, GFR, oddział gdzie przebywa pacjent, zlecone leki cytostatyczne, płyny infuzyjne oraz leki przeciwwymiotne i leki wspomagające. Następnie farmaceuta zatwierdza receptę w specjalnym programie komputerowym i zleca produkcję leku w konkretnej loży. Produkcja powinna się odbywać metodą grawimetryczną tj. przy użyciu programu komputerowego pod kontrolą wagi laboratoryjnej [ryc. 4]. Takie postępowanie pozwala na dokładną dokumentację pobranych dawek leku oraz zapewnienie ciągłości pracy.
Po zakończonej produkcji program drukuje etykietę na przygotowany cytostatyk, którą niezwłocznie należy nakleić na gotowy lek. Etykieta musi zawierać dane takie jak: nazwę apteki, imię i nazwisko pacjenta, datę urodzenia, oddział, nazwę międzynarodową leku oraz nazwę preparatu, dawkę, postać farmaceutyczną, datę sporządzenia, inicjały osoby sporządzającej lek, datę ważności oraz warunki przechowywania preparatu. Gotowy lek cytostatyczny musi być sprawdzony przez personel apteki ze zleceniem lekarskim,
a następnie dostarczony na oddział [ryc. 5].
Proces przygotowywania leku cytostatycznego musi przebiegać w loży z nawiewem laminarnym i z dodatkowym kasetowym filtrem HEPA pod powierzchnią roboczą. Wewnątrz loży zapewniona jest klasa czystości A. W czasie procesu produkcyjnego musi być używany jałowy sprzęt jednorazowego użytku m.in: strzykawki, igły, filtry typu spike, cytoluer, koreczki typu combi, kompresy [ryc.6].
Program komputerowy do produkcji cytostatyków ułatwia pracę zarówno farmaceucie w centralnej pracowni cytostatyków, jak również lekarzom zlecającym chemioterapię i pielęgniarkom potwierdzającym podanie leku. Specjalnie utworzona przez współpracę lekarzy i farmaceutów baza danych pozwala na wybór odpowiednich schematów terapii, wprowadzanie ograniczeń dawek dla konkretnych leków oraz wprowadzanie zasad modyfikacji dawki. Określenie dawki leku jest szczególnie ważne u pacjentów z niewydolnością wątroby, nerek i w przypadku zmian w obrazie krwi. Każdy krok procesu od zaplanowania przez lekarza poprzez weryfikację przez farmaceutę i produkcję cytostatyku aż do podania leku przez pielęgniarkę jest szczegółowo dokumentowany. Dzięki programowi możliwe jest także rozliczenie kosztów zorientowane na pacjenta lub oddział.
Transport leków cytostatycznych na oddział musi odbywać się w zamykanych, nietłukących i wodoszczelnych pojemnikach [6]. Powinny one być zaopatrzone w napisy „ cytostatyki” oraz symbol „ yellow hand” [ryc.7] i napis „ ostrożnie lek silnie działający” [6,9].
Odpady powstałe podczas produkcji cytostatyków są wyrzucane do specjalnego wiaderka koloru żółtego na odpady medyczne, które jest hermetycznie zamykane. Następnie całość wrzucana jest do worka na odpady. Powinien on być odpowiednio opisany specjalnym kodem: 18 01 08 [ryc.8], oznaczającym odpady leków cytostatycznych i cytotoksycznych oraz datą i miejscem ich pochodzenia. Utylizacja i spalenie odpadów następuje według wewnętrznych procedur placówki szpitalnej [10].
Fot. zasoby własne autora
Literatura:
- Ustawa Prawo Farmaceutyczne z dnia 6 września 2001 r. (Dz.U. 2001 Nr 126 poz. 1381 z późn.zm.)
- Prawo farmaceutyczne (Dz.U. z 2008 r. Nr 45. poz. 271)
- Rozporządzenie Ministra Zdrowia z dnia 1 października 2008 r. w sprawie wymagań Dobrej Praktyki Wytwarzania (Dz.U. 2008 nr 184 poz. 1143 z późn. zm.)
- PRZEWODNIK PIC/S W ZAKRESIE DOBRYCH PRAKTYK DOTYCZĄCYCH SPORZĄDZANIA LEKÓW W APTEKACH SZPITALNYCH I ZAKŁADOWYCH
- Rozporządzenie Ministra Zdrowia z dnia 1 października 2008 r. w sprawie wymagań Dobrej Praktyki Wytwarzania (Dz.U. 2008 nr 184 poz. 1143 z późn. zm.)
- Standardy jakościowe w farmacji onkologicnzej QUAPOS 4
- Rozporządzenie Ministra Zdrowia i Opieki Społecznej z dnia 19 czerwca 1996 r. w sprawie bezpieczeństwa i higieny pracy przy przygotowywaniu, podawaniu i przechowywaniu leków cytostatycznych w zakładach opieki zdrwotnej (Dz.U. 1996 nr 80 poz. 376 )
- Standardy Jakościowe w farmacji onkologicznej. K.Chmal – Jagiełło, H Jankowiak – Gracz, M. Bicz, E. Korczowska
- http://www.esop.li/yellowhand_polen.php/
- Rozporządzenie Ministra Zdrowia z dnia 30 lipca 2010 r. w sprawie szczegółowego sposobu postępowania z odpadami medycznymi (Dz.U. 2010 nr 139 poz. 940 )